Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
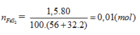
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
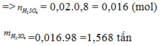

Đáp án C.
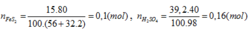
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

Cần bao nhiêu tấn quặng pirit sắt chứa 80% FeS2 để snar xuất 700 tấn dd H2SO4 70% biết rằng hao hụt trong sản xuất là 10%
---
mH2SO4= 700. 70%= 490(tấn)
PTHH: 4 FeS2 + 11 O2 -to,xt-> 2 Fe2O3 + 8 SO2
300_________________________________320(TẤN)
SO2+ 1/2 O2 -to-> SO3
320____________400(TẤN)
SO3 + H2O -> H2SO4
400_________490(TẤN)
mFeS2(LT)= 300(tấn)
-> mFeS2(TT)= (300.100)/90=1000/3 (tấn) (Do dư 10%)
=> m(quặng)= mFeS2(TT)/ 80% = 1000/3 : 80% \(\approx416,7\left(tấn\right)\)

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
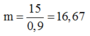


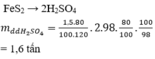



FeS2 --------------> 2H2SO4
120..........................2*98
m...............................100*98%
mFeS2= 98*120/196=60 tấn
mFeS2 (thực có)= 60*100/90= 200/3 tấn
mquặng= 200/3*100/96= 69.44 tấn
Chúc bạn học tốt <3