Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt x,y lần lượt là số mol của MgO và CaO trong hỗn hợp X
vậy hỗn hợp Y có nMgO =x/1,125 mol
=>nHCl =0,57 mol
pu : MgO +2HCl------>MgCl2+H2O
........x........2x...............x
CaO+2HCl------>CaCl2+H2O
y...........2y............y
Vì X'+Na2CO3-------->CO2 nên trong X' có HCl
Na2CO3+2HCl ----->2NaCl+H2O+CO2
0,17........0,085.............................0,17
ta có hệ pt:{2x+2y=0,57−0,17=0,0440x+56y=9,6{2x+2y=0,57−0,17=0,0440x+56y=9,6⇔{x=0,1y=0,1⇔{x=0,1y=0,1
thành phần % của hỗn hợp X là
%m MgO =(0,1*40)*100/9,6=41,67%
%mCaO =58,33%
mX'=9,6+(100*1,047)=114,3g
nồng độ % của các chất trong X '
C% CaCl2 =(0,1*111)*100/114,3=9,71%
C%MgCl2=(0,1*95)*100/114,3=8,31%
C%HCl=(0,17*36,5)*100/114,3=5,43%
b)nMgO (trong Y) =0,089mol ,nAl2O3=(9,6=0,089*40)/102 =0,059 mol
vì nHCl=0,57>2.0,089+6.0,059 =0,532 mol nên hỗn hợp Y bj hòa tan hết
số mol KOH-0,34*2-0,68 mol
trong Y có 0,038 mol HCl
KOH +HCl ----->KCl+Mg(OH)2
0,038...0,038
2KOH+MgCl2 ------>KCl +Mg(OH)2
0,178..0,089......................0,089
3KOH + AlCl3------>3KCl +Al(OH)3
0,354....0,118.........................0,118
lượng KOH dư =0,68 -(0,038+0,178+0,354)=0,11 mol
......Al(OH)3+KOH-------->KAlO2+ 2H2O
BĐ 0,118.....0,11
pu 0,11........0,11
spu 0,08.........0
vậy khôi lượng kết tủa thu đc là m=0,089*58 +0,008*78 =11,362g

\(n_{H_2}=0,2mol\)
2Al+6HCl\(\rightarrow\)2AlCl3+3H2
Fe+2HCl\(\rightarrow\)FeCl2+H2
- Gọi số mol Al là x, số mol Fe là y
- Ta có hệ phương trình:
\(\left\{{}\begin{matrix}27x+56y=5,5\\\dfrac{3}{2}x+y=0,2\end{matrix}\right.\)
Giải ra x=0,1 và y=0,05
%Al=\(\dfrac{0,1.27.100}{5,5}\approx49,1\%\)
%Fe=50,9%
nHCl=3x+2y=0,4mol
\(m_{dd_{HCl}}=\dfrac{0,4.36,5.100}{14,6}=100g\)
\(v_{HCl}=\dfrac{m}{D}=\dfrac{100}{1,12}\approx89,3ml\)
\(C\%_{AlCl_3}=\dfrac{0,1.133,5.100}{5,5+100-0,2.2}=\dfrac{1335}{105,1}\approx12,7\%\)
\(C\%_{FeCl_2}=\dfrac{0,05.127.100}{5,5+100-0,2.2}\approx6,04\%\)

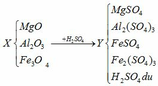
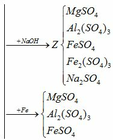
(a) Hòa tan MgO, Al2O3 và Fe3O4 vào H2SO4:
(1) MgO + H2SO4 → MgSO4 + H2O
(2) Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
(3) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
Trung hòa Y:
(4) H2SO4 + 2NaOH → Na2SO4 + 2H2O
Cho dung dịch Y (MgSO4, Al2(SO4)3, FeSO4, Fe2(SO4)3, H2SO4) qua cột chứa bột sắt:
(5) H2SO4 + Fe → FeSO4 + H2
(6) Fe2(SO4)3 + Fe → 3FeSO4
(b) nH2SO4 = 0,45.1 = 0,45 mol
Gọi số mol của MgO, Al2O3 và Fe3O4 trong hỗn hợp ban đầu lần lượt là x, y, z (mol)
Ta có: 40x + 102y + 232z = 20,68 (*)
- Khi hòa tan hỗn hợp vào H2SO4:
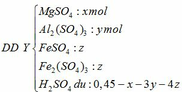
- Trung hòa ¼ dung dịch Y cần 0,025 mol NaOH vậy trung hòa Y cần 0,1 mol NaOH:
Theo PTHH (4): nH2SO4 dư = 0,5nNaOH = 0,05 mol
=> 0,45 – x – 3y – 4z = 0,05
=> x + 3y + 4z = 0,4 (**)
Dung dịch thu được chứa các chất:
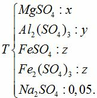
- Giả sử dẫn toàn bộ dung dịch Y qua cột chứa bột Fe:
(5) H2SO4 + Fe → FeSO4 + H2
0,05 → 0,05 (mol)
(6) Fe2(SO4)3 + Fe → 3FeSO4
z → 3z (mol)
Dung dịch sau chứa các chất tan:
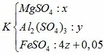
Theo đề bài ta có: mK – mT = 4.1,105
=> [120x + 342y + 152(4z + 0,05)] – [120x + 342y + 152.z + 400z + 0,05.142] = 4,42
=> z = 0,07 (***)
Từ (*) (**) (***) ta giải được z = 0,06; y = 0,02; z = 0,07
Số mol của nguyên tố O trong hỗn hợp X:
nO = nMgO + 3nAl2O3 + 4nFe3O4 = 0,06 + 3.0,02 + 4.0,07 = 0,4 mol
Khối lượng của O: mO = 0,4.16 = 6,4 (gam)
Phần trăm khối lượng của nguyên tố O:


a)
Mg + 2HCl --> MgCl2 + H2
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
MgCl2 + 2KOH + 2KCl + Mg(OH)2
FeCl3 + 3KOH --> 3KCl + Fe(OH)3
Mg(OH)2 --to--> MgO + H2O
2Fe(OH)3 --to--> Fe2O3 + 3H2O
b) Gọi số mol Mg, Fe2O3 là a, b (mol)
Theo PTHH: \(a=n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: \(n_{MgO}=n_{Mg}=a=0,15\left(mol\right)\)
=> \(n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=\dfrac{22-0,15.40}{160}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Fe_2O_3\left(bđ\right)}=n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=0,1\left(mol\right)\)
=> b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{0,15.24+0,1.160}.100\%=18,37\%\\\%m_{Fe_2O_3}=\dfrac{0,1.160}{0,15.24+0,1.160}.100\%=81,63\%\end{matrix}\right.\)


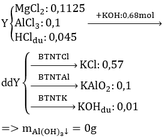

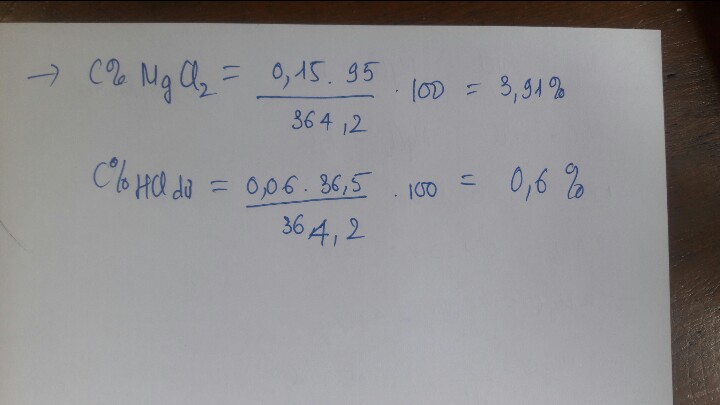

gọi x,y lần lượt là số mol của MgO và CaO trong hỗn hợp X ,số mol của Al2O3 = z
=> hỗn hợp Y có nMgO =\(\frac{x}{1,125}\) mol
=>nHCl =0,57 mol
Xét hỗn hợp X :
MgO + 2HCl = MgCl2+H2O
x 2x
CaO+2HCl = CaCl2+H2O
y 2y
Vì X'+Na2CO3\(\rightarrow\)CO2 nên trong X' có HCl
Na2CO3+2HCl\(\rightarrow\)2NaCl+H2O+CO2
0,17. 0,085 0,17
ta có hệ pt:
\(\begin{cases}2x+2y=0,57-0,17\\40x+56y=9,6\end{cases}\) \(\begin{cases}x=0,1\\y=0,1\end{cases}\)
=> %MgO và %CaO,MgCl2 và CaCl2 , HCl
b)nMgO (trong Y) =0,089mol ,nAl2O3=(9,6-0,089.40)/102 =0,059 mol
vì nHCl=0,57>2.0,089+6.0,059 =0,532 mol nên hỗn hợp Y bj hòa tan hết
nKOH=0,3*2=0,6 mol
trong Y có 0,038 mol HCl
KOH +HCl = KCl+Mg(OH)2
0,038 0,038
2KOH+MgCl2 = KCl +Mg(OH)2
0,178 0,089 0,089
3KOH + AlCl3 = 3KCl +Al(OH)3
0,354 0,118 0,118
=>KOH dư =0,6 -(0,038+0,178+0,354)=0,03 mol
Al(OH)3+KOH = KAlO2+ 2H2O
bđ 0,118 0,03
pu 0,03 0,03
spu 0,088 0
vậy khối lượng kết tủa thu đc là m=0,089.58 +0,088.78 =12,026g
có ai lamf được thi giúp mik cai