Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6

Gọi công thức của A là C a H 2 a của B là C n H 2 n - 2 với a, n > 2, số mol tương ứng cũng là x, y.
Phương trình hóa học:
C n H 2 n - 2 + 2 Br 2 → C n H 2 n - 2 Br 4
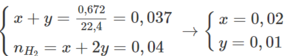
Phương trình hóa học của phản ứng cháy:
C a H 2 a + 3a/2 O 2 → a CO 2 + a H 2 O
C n H 2 n - 2 + (3n-1)/2 O 2 → n CO 2 + (n-1) H 2 O
0,2a + 0,1n = 30,8/44 = 0,7
2a + m = 7 => a = 2; n = 3
Công thức của A là C 2 H 4 của B là C 3 H 4
% V C 2 H 4 = 0,2/0,3 x 100% = 66,67%
% V C 3 H 4 = 33,33%

* Thí nghiệm 1: Cho hỗn hợp X tác dụng với dung dịch Br2
Đặt số mol anken A và ankin B lần lượt là x và y (mol)
nX = x + y = 0,5 (1)
CnH2n + Br2 → CnH2nBr2
x x
CmH2m-2 + 2Br2 → CmH2m-2Br4
y 2y
=> nBr2 = x + 2y = 0,8 (2)
Từ (1) và (2) ta có:
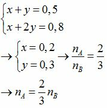
* Thí nghiệm 2: Đốt cháy hỗn hợp X
Hấp thụ CO2 vào dung dịch Ca(OH)2 thấy xuất hiện kết tủa, thêm KOH dư vào dung dịch thu được lại tiếp tục xuất hiện kết tủa nên ta có các phương trình hóa học sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,25 ← 0,25
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 ← 0,025
Ca(HCO3)2 + 2KOH → K2CO3 + CaCO3 + 2H2O
0,025 ← 0,025
nCO2 = 0,25 + 0,05 = 0,3 mol
Ta có: m dung dịch giảm = mCaCO3 – mCO2 – mH2O => 7,48 = 25 – 0,3.44 – mH2O
=> mH2O = 4,32 gam => nH2O = 4,32/18 = 0,24 mol
Mặt khác, nB = nCO2 – nH2O = 0,3 – 0,24 = 0,06 mol
=> nA = 0,06(2/3) = 0,04 mol
BTNT C: nCO2 = n.nA + m.nB => 0,04n + 0,06m = 0,3
=> 2n + 3m = 15 (n≥2, m≥2)
| m |
2 |
3 |
4 |
| n |
4,5 |
3 |
1,5 |
Vậy A là C3H6 và B là C3H4
Khối lượng của hỗn hợp là: m = mC3H6 + mC3H4 = 0,04.42 + 0,06.40 = 4,08 (gam)

có V khí thoát ra = V CnH2n+2 = 2,016 lít
⇒ nCnH2n+2 = 0,09 mol
có nhh =3,136/22,4 =0,14 mol
⇒ nCmH2m = 0,14- 0,09 = 0,05 mol
⇒ %V A = 0,09/0,15 .100% = 60%
%V B = 100% - 60% = 40%
có mdd brom tăng = mCmH2m = 1,4
có m CmH2m = 0,05.14m = 1,4
⇒ n = 2 ( C2H4)
Ca(OH)2 + CO2 ----> CaCO3 + H2O
0,17 0,17 (mol)
Ca(HCO3)2 --to--> CaCO3 + CO2 + H2O
0,05 0,05 (mol)
Ca(OH)2 + 2CO2 ----> Ca(HCO3)2
0,1 0,05 (mol)
⇒ nCO2 = 0,17 +0,1 = 0,27 mol
BTNT Với C :
CnH2n+2 -----> nCO2
0,09 0,09n (Mol)
⇒ 0,09n =0,27
⇒ n = 3
( C3H8)

Khi cho NaOH dư vào thu thêm được kết tủa nên dung dịch có muối Ca(HCO3)2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,5 ← 0,15
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
0,1 ← 0,1
→ nCO2 = 0,1.2 + 0,5 = 0,7
Mặt khác: mdd giảm = mCaCO3 – mCO2 + mH2O
→ 9,12 = 50 – (44.0,7 + 18.nH2O) → nH2O = 0,56

nCO2 = 2,688/22,4 = 0,12 mol; nH2O = 2,52/18 = 0,14 mol
Ta thấy nH2O>nCO2 => ancol là ancol no, đơn chức, mạch hở
Gọi công thức chung của ancol là CkH2k+2O (k €N*)
Giả sử:
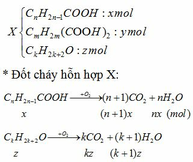
=> nH2O – nCO2 = nx – (n+1)x + (m+1)y – (m+2)y + (k+1)z – kz
=> 0,14 – 0,12 = -x - y + z hay -x - y + z = 0,02 (1)
BTNT ta tính được số mol của các nguyên tố:
nC = nCO2 = 0,12 mol
nH = 2nH2O = 2.0,14 = 0,28 mol
nO = 2nCnH2n-1COOH + 4nCmH2m(COOH)2 + nCkH2k+2O = 2x + 4y + z
=> mX = mC + mH + mO = 0,12.12 + 0,28.1 + 16(2x + 4y + z) = 32x + 64y + 16z + 1,72
* Phản ứng este hóa: Do sau phản ứng chỉ thu được chất có chứa chức este nên axit và ancol phản ứng vừa đủ
n ancol = x + 2y = z hay x + 2y – z = 0 (2)
BTKL ta có: mX = m este + mH2O => 32x + 64y + 16z + 1,72 = 3,22 + 18(x+2y)
hay 14x + 28y + 16z = 1,5 (3)
Từ (1) (2) (3) ta có hệ phương trình:
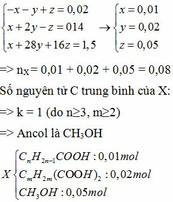
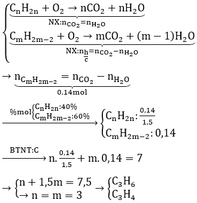
Bảo toàn nguyên tố C ta có: 0,01n + 0,02m + 0,05.1 = 0,12
=> n +2m = 7 mà do n≥3, m≥2 nên chỉ có cặp n = 3, m = 2 thỏa mãn
Vậy các axit trong X là: CH2=CH-COOH và HOOC-COOH.
Kết luận: Hỗn hợp X gồm các chất CH2=CH-COOH, HOOC-COOH và CH3OH.
- Một số ứng dụng của PVC trong thực tế như làm ống dẫn nước, vỏ dây điện, đồ giả da, áo mưa, nhãn chai nước khoáng, …

Phương trình hoá học :
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O
Gọi số mol của hai axit trong hỗn hợp là x.
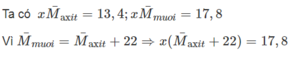
13,4 + 22x = 17,8 => x = 0,2 => số mol của mỗi axit trong hỗn hợp là 0,1
Ta có công thức của 2 axit là C a H 2 a + 1 COOH (0,1 mol)
C b H 2 b + 1 COOH (0,1 mol)
Vậy : (14a + 46)0,1 + (14b + 46)0,1 = 13,4
=> 14a + 14b = 42 => a + b = 3
a = 1; b = 2 → CH 3 COOH và C 2 H 5 COOH
m CH 3 COOH = 0,1 x 60 = 6g
m C 2 H 5 COOH = 0,1 x 74 = 7,4g
% m CH 3 COOH = 6/13,4 x 100% ≈ 44,8%
% m C 2 H 5 COOH = 100% - 44,8% = 55,2%
n NaOH = n CH 3 COOH + n C 2 H 5 COOH = 0,2 mol
V = n : C M = 0,2 : 1 = 200ml

n CO2 = 0,6 mol => m CO2 = 0,6 . 44 = 26,4 g
n H2O = 0,8 mol
=> n ancol = 0,8 – 0,6 = 0,2 mol
Bảo toàn khối lượng : m Oxy + m hỗn hợp = m CO2 + m H2O
=> m oxy + 15,2 = 26,4 + 14,4 => m Oxy = 25,6 g => n O2 = 0,8 mol
Bảo toàn nguyên tố oxy : n O ( trong hỗn hợp ) + 2 n O2 ( đốt cháy ) = n CO2 . 2 + n H2O
=> 2 n axit + n ancol + 0,8 . 2 = 0,8 + 0,6 .2
=> n Axit = 0,1 mol ( vì n ancol = 0,2 mol )
=> n axit . ( n + 1 ) + n ancol . m = n CO2
=> 0,1 . (n + 1 ) + 0,2 . m = 0,6
=> n +2 m = 5
TH1 m = 2 thì n = 1 TH2: m = 1 thì n = 3
C2H5OH và CH3COOH ( loại vì có số C giống nhau đều là 2 C )
hoặc C3H7COOH và CH3OH ( chọn )
C3H7COOH + CH3OH → C3H7COOCH3 + H2O
0,1 0,2 => 0,1 mol
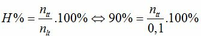
=> n thực tế = 0,09 mol
=> m C3H7COOCH3 = 0,09 . 102 = 9,18 g



a)
\(n_{CO_2} = \dfrac{44}{44} = 1(mol)\\ n_{H_2O} = \dfrac{19,8}{18} = 1,1(mol)\\ n_X = n_{H_2O} - n_{CO_2} = 1,1 -1 = 0,1(mol)\\ \Rightarrow \%V_A = \dfrac{0,1}{0,4}.100\% = 25\%\)
b)
Ctrung bình = \( \dfrac{n_{CO_2}}{n_X} = \dfrac{1}{0,4} = 2,5\)
Suy ra : n < 2,5 < m
Vậy n = 2
A : C2H6 ; B : C2H2
b)
\(n_C = n_{CO_2} = 1\\ n_H = 2n_{H_2O} = 1,1.2 = 2,2\\ \Rightarrow m_X = m_C + m_H = 1.12 + 2,2 = 14,2(gam)\\ \)
Suy ra :
\(m_C = 14,2.39,43\% = 5,6(gam)\\ m_A = 0,1.30 = 3(gam)\\ m_B = 14,2 - 5,6 - 3 = 5,6 \Rightarrow n_B = \dfrac{5,6}{28} = 0,2(mol)\)
nC = nX - nA -nB = 0,4 - 0,1 - 0,2 = 0,1
Suy ra : 0,1.14m = 5,6 ⇒ m = 4 (C4H8)
a)
CnH2n+2 + O2 → nCO2 + (n+1)H2O (1)
CnH2n + O2 → nCO2 + nH2O (2)
CmH2m + O2 → mCO2 + mH2O (3)
Ta thấy khi đốt B và C số mol CO2 thu được bằng số mol H2O
=> Tổng số mol H2O - tổng số mol CO2 = nA
<=> \(\dfrac{19,8}{18}\)- \(\dfrac{44}{44}\)= 0,1 = nA
=> %VA = \(\dfrac{0,1}{0,4}\).100%= 25%
b) Số nguyên tử C trung bình = \(\dfrac{nCO_2}{nX}\)= 2,5
Mà n < m => n = 2
CTPT của A là C2H6 , của B là C2H4
c) Ta có m hỗn hợp X = mC + mH = 1.12 + 1,1.2 = 14,2 gam
=> mC(CmH2m) = mX.39,43% = 5,6 gam
=> mB = mX - mA - mC = 14,2 - 0,1.30 - 5,6 = 5,6 gam
=> nB = \(\dfrac{5,6}{28}\)= 0,2 mol
Mà nX = 0,4 => nC = 0,4 - nA - nB = 0,4 - 0,1 - 0,2 = 0,1 mol
<=> MC = \(\dfrac{5,6}{0,1}\)= 56 (g/mol)
=> 12m + 2m =56 <=> m = 4
Vậy CTPT của C là C4H8