Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
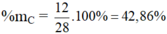
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
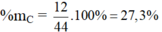
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
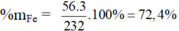
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
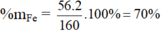
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
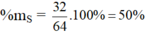
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
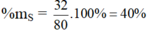
%mO = 100 – 40 = 60%

a/
+ CO
- %mC = \(\frac{12}{12+16}.100\%=42,86\%\)
- %mO = 100% - 42,86% =57,14%
+CO2
- %mC = \(\frac{12}{12+16.2}.100\%=27,27\%\)
- %mO = 100% - 27,27% = 72,73%
b/
+Fe3O4
- %mFe = \(\frac{56.3}{56.3+16.4}.100\%=72,41\%\)
- %mO = 100% - 72,41% = 27,59%
+ Fe2O3
- %mFe = \(\frac{56.2}{56.2+16.3}.100\%=70\%\)
- %mO = 100% - 70% = 30%
c/
+SO2
- %mS = \(\frac{32}{32+16.2}.100\%=50\%\)
- %mO = 100% - 50% = 50%
+ SO3
- %mS = \(\frac{32}{32+16.3}.100\%=40\%\)
- %mO = 100% - 40% = 60%

a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2

SO2 \(\left\{{}\begin{matrix}\%S=\dfrac{32}{64}.100\%=50\%\\\%O=100\%-50\%=50\%\end{matrix}\right.\)
CO2 \(\left\{{}\begin{matrix}\%C=\dfrac{12}{44}.100\%=27,27\%\\\%O=100\%-27,27\%=72,73\%\end{matrix}\right.\)
H2O \(\left\{{}\begin{matrix}\%H=\dfrac{2}{18}.100\%=11,11\%\\\%O=100\%-11,11\%=88,89\%\end{matrix}\right.\)

4.
a) \(V_{SO_2}=0.5\cdot22.4=11.2\left(l\right)\)
b) \(V_{CH_4}=\dfrac{3.2}{16}\cdot22.4=4.48\left(l\right)\)
c) \(V_{N_2}=\dfrac{0.9\cdot10^{23}}{6\cdot10^{23}}\cdot22.4=3.36\left(l\right)\)
5.
a) \(m_{Al}=0.1\cdot27=2.7\left(g\right)\)
b) \(m_{Cu\left(NO_3\right)_2}=0.3\cdot188=56.4\left(g\right)\)
c) \(m_{Na_2CO_3}=\dfrac{1.2\cdot10^{23}}{6\cdot10^{23}}\cdot106=21.2\left(g\right)\)
d) \(m_{CO_2}=\dfrac{8.96}{22.4}\cdot44=17.6\left(g\right)\)
e) \(m_K=0.5\cdot2\cdot39=39\left(g\right)\\ m_C=0.5\cdot12=6\left(g\right)\\ m_O=0.5\cdot3\cdot16=24\left(g\right)\)

nCO2 = 0,03 mol → nC = nCO2 = 0,03 mol
nH2O = 0,06 mol → nH = 2nH2O = 0,12 mol
mN = 1,8.46,67% = 0,84 gam → nN = 0,84/14 = 0,06 mol
→ mO = mA - mC - mH - mN = 1,8 - 0,03.12 - 0,12 - 0,06.14 = 0,48 gam
→ nO = 0,48/16 = 0,03 mol
→ C : H : O : N = 0,03 : 0,12 : 0,03 : 0,06 = 1 : 4 : 1 : 2
→ CTPT có dạng (CH4ON2)n
Mà N trong 1 mol A ít hơn N trong 100 gam NH4NO3 nên ta có:
2n < 2.(100/80) → n < 1,25
→ n = 1
→ CTPT là CH4ON2 hay (NH2)2CO
Tên gọi của A là ure

\(^M\)\(k2CO3\)\(=39,2+12,1+16,3\)\(=138g\)/mol
Trong 1 mol K2CO3 có: 2 mol nguyên tử K
%mK=\(\dfrac{39.2.100\text{ %}}{138}\)=56,52 %


\(\%_{Na_{\left(Na_2CO_3\right)}}=\dfrac{23.2}{23.2+12+16.3}.100\%\approx43,4\%\)
\(\%_{C_{\left(Na_2CO_3\right)}}=\dfrac{12}{23.2+12+16.3}.100\%\approx11,3\%\)
\(\%_{O_{\left(Na_2CO_3\right)}}=100\%-43,4\%-11,3\%=45,3\%\)
(Các chất còn lại tương tự.)