Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

B
X và Y là hai kim loại cùng nhóm A.
=> Y có nhiều hơn X là 8 hoặc 18 hoặc 32 electron.
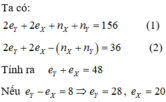
(không thuộc 2 chu kì)(loại).
![]()
Vậy 2 nguyên tố này là As và P, cùng thuộc nhóm VA và thuộc 2 chu kì (nhận).
![]()
(không thuộc 2 chu kì liên tiếp) (loại).
Vậy X là photpho (P).

Đáp án C
Vì X và Y thuộc cùng một nhóm A và ở chu kì liên tiếp nên ta có:
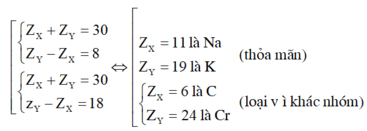
Khi đó cấu hình electron là của Na là 1s22s22p63s1

Đáp án C
Vì X và Y thuộc cùng một nhóm A và ở chu kì liên tiếp nên ta có:
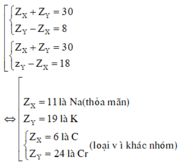
Khi đó cấu hình electron là của Na là 1s22s22p63s1.

Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
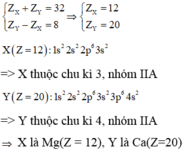
Trường hợp 2:
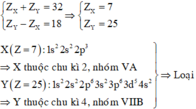
Trường hợp 3:
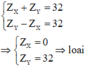

Đáp án C
Theo đề bài, ta có: ZX + ZY = 22 (1)
- Nếu X, Y thuộc hai chu kì nhỏ thì (ZX < ZY): ZY = ZX + 8 (2)
Từ (1) và (2) => ZX =7; ZY = 15.
Vậy X là N, Y là P
- Nếu X thuộc chu kì nhỏ và Y thuộc chu kì lớn thì: ZY = ZX + 18 (3)
Từ (1) và (3) => ZX = 2; ZY = 20 (loại vì không thảo mãn đề bài)
- Nếu X, Y thuộc hai chu kì lớn: ZY = ZX + 32 (4)
Từ (1) và (4) => ZX <0 (loại)

Giả sử pX < pY
Do X, Y thuộc 2 nhóm A liên tiếp trong cùng 1 chu kì
=> pY - pX = 1
Có pX + pY = 33
=> pX = 16, pY = 17
=> Số hiệu nguyên tử của X là 16, của Y là 17


