Tính khối lượng đồng Cu có trong 64g đồng sunfat CuSO4?
nhanh vs ạ cần gấp!!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(V_{dd}=165,84\left(ml\right)=0,16584\left(l\right)\\ n_{CuSO_4}=\dfrac{36}{160}=0,225\left(mol\right)\\ \rightarrow C_{M\left(CuSO_4\right)}=\dfrac{0,225}{0,16584}=1,36M\)

a/ \(m_{Cu}=\dfrac{I.A_{Cu}.t}{F.n_{Cu}};m_{Ag}=\dfrac{I.A_{Ag}.t}{F.n_{Ag}}\)
\(m_{Cu}+m_{Ag}=2,8\Leftrightarrow\dfrac{I.64.t}{96500.2}+\dfrac{I.108.t}{96500.1}=2,8\)
\(\Rightarrow q=I.t=2,8.\dfrac{4825}{7}=1930\left(C\right)\)
\(\Rightarrow m_{Cu}=\dfrac{1930.64}{96500.2}=...\left(g\right);m_{Ag}=\dfrac{1930.108}{96500}=...\left(g\right)\)
b/ \(q=I.t=1930\Rightarrow t=\dfrac{1930}{0,5}=3860\left(s\right)\)

\(PTHH:Cu+Cl_2\xrightarrow{t^o} CuCl_2\\ \Rightarrow n_{Cu}=n_{CuCl_2}=n_{Cl_2}=0,1(mol)\\ \Rightarrow m_{Cu}=0,1.64=6,4(g); m_{CuCl_2}=0,1.135=13,5(g)\)

$n_{CuSO_4} = 2(mol)$
$n_{CuSO_4\ dư} = 2.0,8 = 1,6(mol)$
$\Rightarrow n_{CuSO_4\ pư} = 2 - 1,6 = 0,4(mol)$
$Fe + CuSO_4 \to FeSO_4 + Cu$
Theo PTHH :
$n_{Fe} = n_{CuSO_4\ pư} = 0,4(mol)$
$m_{Fe} = 0,4.56 = 22,4(gam)$

Bài 2: PTHH: FeO + 2HCl → FeCl2 + H2O
Fe + 2HCl → FeCl2 + H2 ↑
Số mol của H2 là: 2,24 : 22,4 = 0,1 mol
Số mol của Fe là: 0,1 mol
Khối lượng của Fe trong hỗn hợp là: 0,1 . 56 = 5,6 gam
1) btoàn klg=>mCO2=mcr ban đầu-m cr sau=20-15,6=4,4 gam
=>nCO2=0,1 mol
=>VCO2=2,24 lit

Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
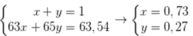
Phần trăm khối lượng của 63Cu trong CuSO4 là
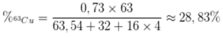

\(M_{CuSO4.nH2O}=25,6.64=250\)
\(M_{\left(H2O\right)n}=250-160=90\left(\frac{g}{mol}\right)\)
\(\Rightarrow n=\frac{90}{18}=5\)

\(\left\{{}\begin{matrix}m_{Fe}=1,68g;M_{Fe}=56g\\SốmolFe.n_{Fe}=\dfrac{n}{M}=\dfrac{1,68}{56}=0,03mol\end{matrix}\right.\)
Pt: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\downarrow\)
\(0,03mol\rightarrow0,03mol\)
\(\left\{{}\begin{matrix}n_{Cu\downarrow}=0,03mol;M_{Cu}=64\\\Rightarrow khốilượngCu.m_{Cu}=n.M=0,03.64=1,92\left(gam\right)\end{matrix}\right.\)
PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\downarrow\)
Ta có:\(n_{Fe}=\dfrac{1,68}{56}=0,03\left(mol\right)\)
=> \(n_{Cu}=n_{Fe}=0,3\left(mol\right)\\ \rightarrow m_{Cu}=0,3.64=19,2\left(g\right)\)
Cách 1: Ta có: \(n_{CuSO_4}=\dfrac{64}{160}=0,4\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,4.64=25,6\left(g\right)\)
Cách 2:
Ta có: \(\%m_{Cu}=\dfrac{64}{64+32+16.4}.100\%=40\%\)
\(\Rightarrow m_{Cu}=64.40\%=25,6\left(g\right)\)
Bạn tham khảo nhé!
e cảm ơn ạ