Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$PTHH:Zn+2HCl\to ZnCl_2+H_2\uparrow$
$n_{Zn}=\dfrac{13}{65}=0,2(mol)$
Theo PT: $n_{ZnCl_2}=n_{H_2}=0,2(mol);n_{HCl}=0,4(mol)$
$a)m_{axit}=m_{HCl}=n.M=0,4.36,5=14,6(g)$
$b)m_{ZnCl_2}=n.M=0,2.136=27,2(g)$
$c)V_{H_2(đktc)}=n.22,4=0,2.22,4=4,48(lít)$
Số mol kẽm là :
\(n=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH : Zn + 2HCL -> ZnCl2 + H2
1 2 1 1
0,2 mol -> 0,4 mol 0,2 mol 0,2 mol
a, Khối lượng HCL là :
\(m=n.M=0,4.35,5=14,2\left(g\right)\)
b, Khối lượng ZnCL2 là :
\(m=n.M=0,1.136=13,6\left(g\right)\)
c, Thể tích H2 là : V = n . 22,4 = \(0,1.22,4=2,24\left(l\right)\)

Ta có: \(n_{H_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
a, \(n_{Mg}=n_{H_2}=0,3\left(mol\right)\Rightarrow m_{Mg}=0,3.24=7,2\left(g\right)\)
b, \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)
c, Cách 1: \(n_{MgCl_2}=n_{H_2}=0,3\left(mol\right)\Rightarrow m_{MgCl_2}=0,3.95=28,5\left(g\right)\)
Cách 2: Theo ĐLBT KL, có: mMg + mHCl = mMgCl2 + mH
⇒ mMgCl2 = 7,2 + 21,9 - 0,3.2 = 28,5 (g)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, Theo PT: \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)

a)
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
b) $n_{HCl} = 2n_{H_2} = 0,3(mol)$
$\Rightarrow m_{HCl} = 0,3.36,5 = 10,95(gam)$
c)
Cách 1 : $n_{FeCl_2} = n_{H_2} = 0,15(mol) \Rightarrow m_{FeCl_2} = 0,15.127 = 19,05(gam)$
Cách 2 : Bảo toàn khối lượng, $m_{FeCl_2} = 8,4 + 10,95 - 0,15.2 = 19,05(gam)$

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
+\(n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
+\(nH_2=n_{Zn}=0,5\left(mol\right)\)
+\(n_{HCl}=2n_{Zn}=1\left(mol\right)\)
+\(V_{H2}=0,5.22,4=11,2\left(lit\right)\)
\(m_{HCl}=1.36,5=36,5\left(gam\right)\)
\(n_{Zn}=\dfrac{m}{M}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
\(Zn\) \(+\) \(2\)\(HCl\) → \(ZnCl_2\) \(+\) \(H_2\)
\(0,5\) \(mol\) → \(1\) \(mol\) → \(0,5\)\(mol\) → \(0,5\) \(mol\)
\(V_{H_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
\(m_{HCl}=n.M=1.36,5=36,4\left(g\right)\)

\(nZn=\dfrac{6,5}{65}=0,1mol\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1--->0,2------->0,2------>0,1
a, \(VH_2=0,1.22,4=2,24lít\)
b, \(mHCl=0,2.36,5=3,65g\)
c, cách 1:
\(mZnCl_2=0,2.136=27,2gam\)
cách 2 :
\(mH_2=0,1.2=0,2gam\)
BTKL: mZn+mHCl=mZnCl2+H2
6,5+3,65 =mZnCl2+0,2
sao cái cách 2 btkl mình cs tính kq mà s nhìn nó lạ lắm

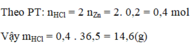

PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
___0,3____0,6_____0,3____0,3 (mol)
a, \(m_{Zn}=0,3.65=19,5\left(g\right)\)
b, \(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
c, \(m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
Bạn tham khảo nhé!
Zn+2HCl->ZnCl2+H2
0,3---0,6-----0,3----0,3 mol
=>m Zn=0,3.65=19,5g
=>m HCl=0,6.35,6=21,9g
=>m ZnCl2=0,3.136=40,8g